रासायनिक अभिक्रिया एवं समीकरण : NCERT Science Class 10
विचार कीजिए कि क्या होता है जब
🔹 गर्मियों में कमरे के ताप पर दूध को खुला छोड़ दिया जाता है।
🔹 लोहे का तवा/तसला/कील को नम वायुमंडल में खुला छोड़ दिया जाता है।
🔹 भोजन को पकाया जाता है।
🔹 हमारा शरीर भोजन को पचा लेता है।
🔹 हम साँस लेते हैं।
इन सभी परिस्थितियों में प्रारंभिक वस्तु की प्रकृति तथा पहचान कुछ न कुछ बदल जाती है। इसका मतलब है कि इन सबमें कहीं न कहीं कोई रासायनिक परिवर्तन हुआ है औऱ जब कोई रासायनिक परिवर्तन होता है तो हम कहते हैं कि एक रासायनिक अभिक्रिया हुई है।
हम कैसे जान सकते हैं कि कोई रासायनिक अभिक्रिया हुई है? इन प्रश्नोें के उत्तर पाने के लिए आइए हम कुछ क्रियाकलाप करते हैं।
क्रियाकलाप 1.1
सावधानीः इस क्रियाकलाप में शिक्षक के सहयोग की आवश्यकता है। सुरक्षा के लिए छात्र आँखों पर चश्मा पहन लें तो उचित होगा।
🔹 लगभग 3-4 cm लंबे मैग्नीशियम रिबन को रेगमाल से रगड़कर साफ़ कर लीजिए।
🔹 इसे चिमटे से पकड़कर स्पिरिट लैंप या बर्नर से इसका दहन करिए तथा इससे बनी राख को वॉच ग्लास में इकट्ठाकर लीजिए जैसा कि चित्र 1.1 में दिखाया गया है। मैग्नीशियम रिबन का दहन करते समय इसे अपनी आँखों से यथासंभव दूर रखिए।
🔹आपने क्या प्रेक्षण किया?
चित्र 1.1
मैग्नीशियम रिबन का वायु में दहन कर मैग्नीशियम अॉक्साइड को वॉच ग्लास में इकट्ठा करना
चमकदार श्वेत ज्वाला के साथ मैग्नीशियम रिबन जलता है और यह श्वेत चूर्ण में परिवर्तित हो जाता है। यह मैग्नीशियम अॉक्साइड का चूर्ण है। वायु में उपस्थित अॉक्सीजन तथा मैग्नीशियम के बीच होने वाली अभिक्रिया के कारण यह बनता है।
क्रियाकलाप 1.2
🔹 एक शंक्वाकार फ़्लास्क या परखनली में कुछ दानेदार जिंक लीजिए।
🔹 इसमें तनु हाइड्रोक्लोरिक अम्ल या सल्फ़्यूरिक अम्ल मिला दीजिए
सावधानीः अम्ल का इस्तेमाल सावधानी से कीजिए।
🔹 क्या जस्ते के दानों के आसपास कुछ होता दिखाई दे रहा है?
🔹 शंक्वाकार फ्लास्क या परखनली को स्पर्श कीजिए। क्या इसके तापमान में कोई परिवर्तन हुआ है?
चित्र 1.2 दानेदार जस्ते पर तनु सल्फ़्यूरिक अम्ल की अभिक्रिया से हाइड्रोजन गैस का निर्माण
इन क्रियाकलापों के अधार पर हम किसी भी प्रेक्षण की सहायता से बता सकते हैं कि एक रासायनिक अभिक्रिया हुई है या नहीं ।-
🔺अवस्था में परिवर्तन
🔺 रंग में परिवर्तन
🔺गैस का निकास/उत्सर्जन
🔺 तापमान में परिवर्तन
यदि हम अपने आसपास हो रहे परिवर्तनों को देखें, तो पाएँगे कि हमारे चारों ओर विविध प्रकार की रासायनिक अभिक्रियाएँ हो रही हैं।
रासायनिक समीकरण
क्रियाकलाप 1.1 का विवरणः
जब अॉक्सीजन की उपस्थिति में मैग्नीशियम रिबन का दहन होता है तब यह मैग्नीशियम अॉक्साइड में परिवर्तित हो जाता है। वाक्य के रूप में किसी रासायनिक अभिक्रिया का विवरण बहुत लंबा हो जाता है। इसे संक्षिप्त रूप में भी लिखा जा सकता है। इसे शब्द-समीकरण के रूप में लिखना सबसे सरलतम विधि है।
ऊपर दी गई अभिक्रिया का शब्द-समीकरण इस प्रकार होगाः
मैग्नीशियम + अॉक्सीजन → मैग्नीशियम अॉक्साइड (1.1)
(अभिकारक) (उत्पाद)
अभिक्रिया (1.1) में मैग्नीशियम तथा अॉक्सीजन एेसे पदार्थ हैं जिनमें रासायनिक परिवर्तन होता है, इन्हें अभिकारक कहते हैं। इस अभिक्रिया से एक नए पदार्थ मैग्नीशियम अॉक्साइड का निर्माण होता है, इसे उत्पाद कहते हैं।
शब्द-समीकरण में अभिकारकों के उत्पाद में परिवर्तन को उनके मध्य एक तीर का निशान लगाकर दर्शाया जाता है। अभिकारकों के बीच योग (+) का चिह्न लगाकर उन्हें बाईं ओर (LHS) लिखा जाता है। इसी प्रकार उत्पादों के बीच भी योग (+) का चिह्न लगाकर उन्हें दाईं ओर (RHS) लिखा जाता है। तीर का सिरा उत्पाद की ओर होता है तथा यह अभिक्रिया होने की दिशा को दर्शाता है।
रासायनिक समीकरण लिखना
क्या रासायनिक समीकरण के निरूपण की इससे भी संक्षिप्त विधि है? शब्दों की जगह रासायनिक सूत्र का उपयोग करके रासायनिक समीकरणों को अधिक संक्षिप्त तथा उपयोगी बनाया जा सकता है। रासायनिक समीकरण किसी रासायनिक अभिक्रिया को दर्शाता है। यदि आप मैग्नीशियम, अॉक्सीजन तथा मैग्नीशियम अॉक्साइड के सूत्रों का स्मरण करें तो उपरोक्त शब्द-समीकरण इस प्रकार लिखा जा सकता हैः
Mg + O2 → MgO (1.2)
तीर के निशान के बाईं और दाईं ओर के तत्वों के परमाणुओं की संख्या की गिनती कर उनकी तुलना करें। क्या दोनों ओर तत्वों के परमाणुओं की संख्या समान है? यदि है, तो समीकरण संतुलित है। यदि नहीं, तो समीकरण असंतुलित है क्योंकि समीकरण के दोनों ओर का द्रव्यमान बराबर नहीं है। किसी अभिक्रिया का एेसा रासायनिक समीकरण ढाँचा रासायनिक समीकरण कहलाता है। इस प्रकार समीकरण (1.2) मैग्नीशियम के वायु में जलने का ढाँचा समीकरण है।
संतुलित रासायनिक समीकरण का महत्व
द्रव्यमान के संरक्षण के नियम के अनुसार किसी भी रासायनिक अभिक्रिया में द्रव्यमान का न तो निर्माण होता है न ही विनाश। अर्थात किसी भी रासायनिक अभिक्रिया के उत्पाद तत्वों का कुल द्रव्यमान अभिकारक तत्वों के कुल द्रव्यमान के बराबर होता है।
दूसरे शब्दों में, रासायनिक अभिक्रिया के पहले एवं उसके पश्चात प्रत्येक तत्व के परमाणुओं की संख्या समान रहती है। इसलिए हमें समीकरण को संतुलित करना आवश्यक है। क्या रासायनिक समीकरण (1.2) संतुलित है? आइए हम रासायनिक समीकरण को चरणबद्ध संतुलित करना सीखें।
क्रियाकलाप 1.2 के शब्द-समीकरण को इस प्रकार दर्शाया जा सकता हैः
जिंक + सल्फ़्यूरिक अम्ल → जिंक सल्फ़ेट + हाइड्रोजन
उपरोक्त शब्द-समीकरण को निम्नलिखित रासायनिक समीकरण से दर्शाया जा सकता हैः
Zn + H2SO4 → ZnSO4 + H2 (1.3)
आइए, समीकरण (1.3) में तीर के निशान के दोनों ओर के तत्वों के परमाणुओं की संख्या की तुलना करें।
समीकरण (1.3) में, तीर के निशान के दोनों ओर के प्रत्येक तत्व के परमाणुओं की संख्या समान है इसलिए यह एक संतुलित रासायनिक समीकरण है।
अब हम निम्न रासायनिक समीकरण को संतुलित करने का प्रयास करते हैंः
Fe + H2O → Fe3O4 + H2 (1.4)
चरण 1 🔸 रासायनिक समीकरण को संतुलित करने के लिए सबसे पहले प्रत्येक सूत्र के चारों ओर एक बॉक्स बना लीजिए। समीकरण को संतुलित करते समय बॉक्स के अंदर कुछ भी परिवर्तन नहीं कीजिए।
Fe + H2O → Fe3O4 + H2 (1.5)
चरण 2 🔸 असंतुलित समीकरण (1.5) में उपस्थित विभिन्न तत्वों के परमाणुओं की संख्या की सूची बना लीजिए।
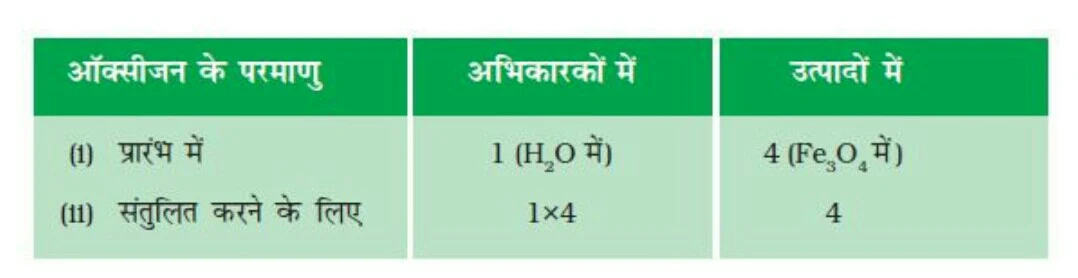
चरण 3 🔸 सुविधा के लिए सबसे अधिक परमाणु वाले यौगिक को पहले संतुलित कीजिए चाहे वह अभिकारक हो या उत्पाद। उस यौगिक में सबसे अधिक परमाणु वाले तत्व को चुनिए। इस आधार पर हम Fe3O4 और उसके अॉक्सीजन तत्व को चुनते हैं। दाईं ओर अॉक्सीजन के चार परमाणु हैं जबकि बाईं ओर केवल एक।
अॉक्सीजन परमाणु को संतुलित करने के लिएः
यह याद रखना आवश्यक है कि परमाणुओं की संख्या को बराबर करने के लिए हम अभिक्रिया में शामिल तत्वों तथा यौगिकों के सूत्रों को नहीं बदल सकते हैं। जैसे कि अॉक्सीजन परमाणु को संतुलित करने के लिए हम ‘4’ गुणांक लगाकर 4 H2O लिख सकते हैं लेकिन H2O4 या (H2O)4 नहीं। आंशिक रूप से संतुलित समीकरण अब इस प्रकार होगाः
Fe + 4 H2O → Fe3O4 + H2
चरण 4 🔸 Fe तथा H परमाणु अब भी संतुलित नहीं हैं। इनमें से किसी एक तत्व को चुनकर आगे बढ़ते हैं। अब हम आंशिक रूप से संतुलित समीकरण में हाइड्रोजन परमाणु को संतुलित करते हैंः
हाइड्रोजन परमाणु को बराबर करने के लिए दाईं ओर हाइड्रोजन अणु की संख्या को ‘4’ कर देते हैं।
समीकरण अब इस प्रकार होगाः
Fe + 4 H2O → Fe3O4 + 4 H2
चरण 5 🔸 ऊपर दिए समीकरण की जाँच कीजिए तथा तीसरा तत्व चुन लीजिए जो अब तक असंतुलित है। आप पाएँगे कि केवल लोहा ही एक तत्व है जिसे संतुलित करना शेष है।
Fe को संतुलित करने के लिए बाईं ओर हम Fe के 3 परमाणु लेते हैं।
3 Fe + 4 H2O → Fe3O4 + 4 H2 (1.8)
चरण 6 🔸 अंत में, इस संतुलित समीकरण की जाँच के लिए हम समीकरण में दोनों ओर के तत्वों के परमाणुओं की संख्याओं का परिकलन करते हैं।
3 Fe + 4H2O → Fe3O4 + 4 H2 (1.9)
समीकरण (1.9) में दोनों ओर के तत्वों के परमाणुओं की संख्या बराबर है। अतः यह समीकरण अब संतुलित है। रासायनिक समीकरणों को संतुलित करने की इस विधि को हिट एंड ट्रायल विधि कहते हैं क्योंकि सबसे छोटी पूर्णांक संख्या के गुणांक का उपयोग करके समीकरण को संतुलित करने का प्रयत्न करते हैं।
चरण 7 🔸 भौतिक अवस्थाओ के संकेत लिखनाः ऊपर लिखे संतुलित समीकरण (1.9) की सावधानी से जाँच कीजिए। क्या इस समीकरण से हमें अभिकारकों तथा उत्पादों की भौतिक अवस्था के बारे में भी ज्ञान होता है? इस समीकरण में उनकी भौतिक अवस्थाओं की कोई जानकारी नहीं है।
रासायनिक समीकरण को अधिक सूचनापूर्ण बनाने के लिए अभिकारकों तथा उत्पादों के रासायनिक सूत्र के साथ उनकी भौतिक अवस्था को भी दर्शाया जाता है। अभिकारकों तथा उत्पादों के गैस, द्रव, जलीय तथा ठोस अवस्थाओं को क्रमशः (g), (l), (aq) तथा (s) से दर्शाया जाता है। अभिकारक या उत्पाद जब जल में घोल के रूप में उपस्थित होते हैं तब हम (aq) लिखते हैं।
अब संतुलित समीकरण (1.9) इस प्रकार होगाः
3Fe(s) + 4H2O(g) → Fe3O4(s) + 4H2(g) (1.10)
ध्यान दीजिए समीकरण (1.10) में H2O के साथ (g) चिह्न का उपयोग किया गया है। यह दर्शाता है कि इस अभिक्रिया में जल का उपयोग भाप के रूप में किया गया है।
प्रायः हर रासायनिक समीकरण में भौतिक अवस्था को शामिल नहीं किया जाता है, जब तक कि यह आवश्यक न हो।
कभी-कभी अभिक्रिया की परिस्थितियाँ जैसे कि ताप, दाब, उत्प्रेरक आदि को भी तीर के निशान के ऊपर या नीचे दर्शाया जाता है। जैसे,
अब इन प्रश्नों के उत्तर देने का प्रयास कीजिए-
1. वायु में जलाने से पहले मैग्नीशियम रिबन को साफ़ क्यों किया जाता है?
2. निम्नलिखित रासायनिक अभिक्रियाओं के लिए संतुलित समीकरण लिखिएः
(i) हाइड्रोजन + क्लोरीन → हाइड्रोजन क्लोराइड
(ii) बेरियम क्लोराइड + एेलुमीनियम सल्फ़ेट → बेरियम सल्फ़ेट + एेलुमीनियम क्लोराइड
(ii) सोडियम + जल → सोडियम हाइड्रॉक्साइड + हाइड्रोजन
3. निम्नलिखित अभिक्रियाओं के लिए उनकी अवस्था के संकेतों के साथ संतुलित रासायनिक समीकरण लिखिएः
(i) जल में बेरियम क्लोराइड तथा सोडियम सल्फ़ेट के विलयन अभिक्रिया करके सोडियम क्लोराइड का विलयन तथा अघुलनशील बेरियम सल्फ़ेट का अवक्षेप बनाते हैं।
(i) सोडियम हाइड्रोक्साइड का विलयन (जल में) हाइड्रोक्लोरिक अम्ल के विलयन (जल में) से अभिक्रिया करके सोडियम क्लोराइड का विलयन तथा जल बनाते हैं।










Comments
Post a Comment